Bu yazıda periyodik tablo hakkında bilinmesi gereken temel bilgiler ve atomların elektron dağılımıyla ilgili bilgiler özet halinde verilmektedir.
- Periyodik cetveldeki yatay sıralara periyot,
- Dikey sıralara Grup
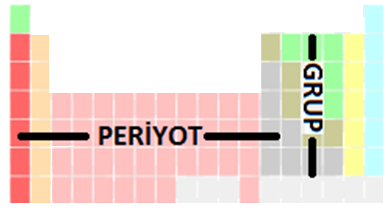
- Periyodik tabloda elementler atom numaralarına göre sıralanır.

- Periyodik tablonun temellerini atan bilim insanı Mendeleyev’dir.
- Bazı grupların özel isimleri:
1A : Alkali metaller
2A: Toprak alkali metalleri
7A: Halojenler
8A: Soygazlar - Grup ve periyot numarasını bulma
Atom numarası bilinen elementin elektron dağılımı yapılır. Son katmandaki elektron sayısı grup numarasını, toplam katman sayısı periyot numarasını verir.
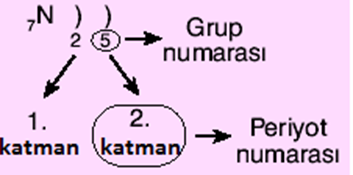
- Atomun iyon yükünü bulma.11Na : elektron dağılımı
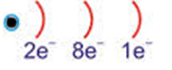
Son katmandaki 1e verir. Elektron verenler + yüklenir +1 yüklü olur.
17Cl: Klorun elektron dağılımı
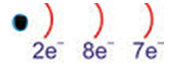
Son katmanında 1 elektron eksik olduğu için 1e alır ve -1 yüklü olur.
- Anyon ve katyonlar
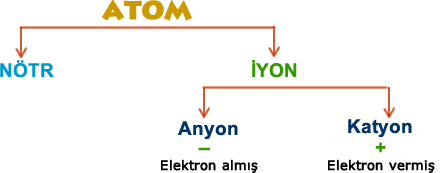
- Periyodik tablodaki grupların iyon değerleri
1A: +1
2A: +2
3A: +3
4A:+ – 4
5A: -3
6A: -2
7A: -1
8A: Değerlik almaz - Değerlik elektron sayısı
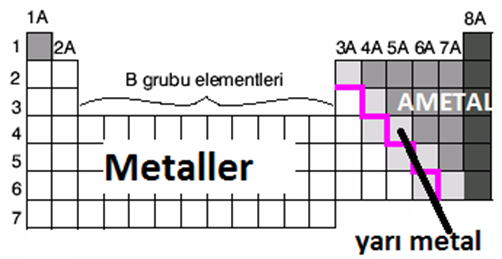
Bir atomun son katmanındaki elektron sayısına denir. - Metal, Ametal ve Yarı Metallerin yeri
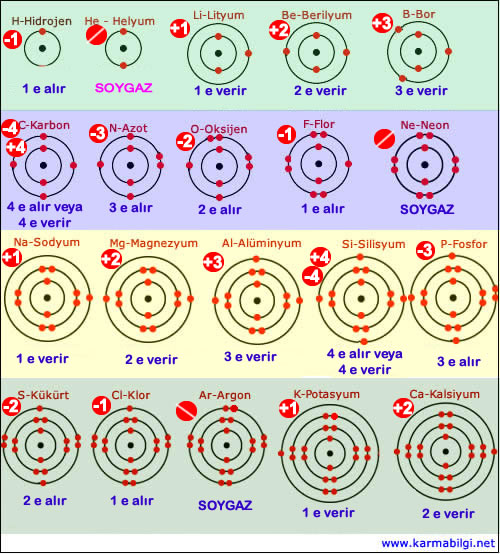
İlk yirmi elementin elektron dağılımı ve iyon yükleri
- Metallerin Özellikleri
1- Katıdırlar ( Civa = Hg hariç )
2- Yüzeyleri parlaktır3- Isı ve elektriği iyi iletirler
4- Tel ve levha haline gelebilirler
5- Tek atomludurlar ( atomik yapılıdırlar )
6- Kendi aralarında bileşik yapmazlar
7- Kendi aralarında alaşım yaparlar
8- Elektron verme özelliğindedirler ( katyon = +)
9- Ametallerle iyonik bileşik yaparlar
10- Canlıların yapısında çok az bulunur
11- Erime-kaynama noktaları yüksektir
12- 1A,2A,3A grubunda bulunurlar
13- Sulu çözeltileri BAZ özelliği taşı
14- Periyodik tablonun sol tarafındadırlar
- Ametallerin Özellikleri
1- Katı, sıvı, gaz halindedirler
2- Yüzeyleri mattır
3- Isı ve elektriği iyi iletmezler
4-Tel ve levha haline gelemezler
5- İki ve daha fazla atomludurlar ( molekül yapılı)
6- Kendi aralarında bileşik yaparlar
7- Kendi aralarında alaşım yapmazlar
8- Elektron alma özelliğindedirler ( Anyon= – )
9- Kendi aralarında Kovalent bileşik yaparlar
10- Canlıların yapısında bolca bulunurlar
11- Erime-kaynama noktaları düşüktür
12- 4A,5A,6A,7A grubunda bulunurlar
13- Sulu çözeltileri ASİT özelliği taşır.
14- Periyodik tablonun sağ tarafındadırar.
- Yarı Metallerin Özellikleri
1- Parlak veya mat olabilirler
2-Elektrik ve ısıyı ametallerden daha iyi metallerden daha az iletirler.
3- İşlenebilirler ( tel ve levha haline getirilebilirler )
4- Kırılgan değildirler.
